- КАЛЕНДАР АКТИВНОСТИ
- ОРГАНИЗАЦИЈА РАДА ШКОЛЕ
- ВЕСТИ
- РАСПОРЕД ПИСМЕНИХ ПРОВЕРА I ЦИКЛУС
- РАСПОРЕД ПИСМЕНИХ ПРОВЕРА II ЦИКЛУС
- ТАКМИЧЕЊА
- ЕКСКУРЗИЈЕ И НАСТАВА У ПРИРОДИ
- ЂАЧКИ КУТАК
- КОНСУЛТАЦИЈЕ - ТЕРМИНИ
- ПРЕУЗИМАЊЕ
- ПОСЛОВНИЦИ И СТАТУТИ
- PRAVILNICI
- СТАНДАРДИ
- ПЕДАГОШКО-ПСИХОЛОШКА СЛУЖБА
- ЛЕТОПИС
- ДОДАТНА ПОДРШКА РОДИТЕЉИМА ПРИ ДИГИТАЛИЗАЦИЈИ
- НАШИ ЧАСОВИ НА РТС-У
- ПРОГРАМ ТАКМИЧЕЊА ИЗ МАТЕМАТИКЕ
ОШ "ЉУБИША УРОШЕВИЋ" - Рибаре
ризница знања ...
ризница знања ...
 |
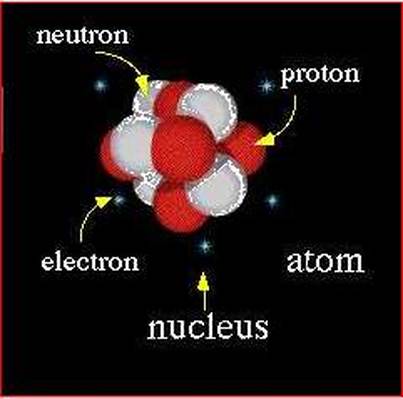
Структура атома. Нуклеарне силе
Страна у припреми
Извор fizikazaosnovce678